Ces propriétés extraordinaires de l'eau auxquelles nous devons la vie
Plus on avance dans la compréhension du vivant, de l'écologie et des exoplanètes, plus on découvre l'importance de l'eau, un corps pur particulièrement singulier. Comparée aux autres molécules minérales, celle de l'eau est une championne toutes catégories.
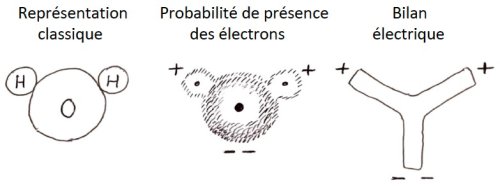
Ses qualités tiennent grandement à la forme que prend son nuage électronique. L'oxygène attire très fortement les électrons. Au contraire, les atomes d'hydrogène ont tendance à s'en défaire. De cette complémentarité résulte une forte asymétrie : les électrons se localisent très majoritairement du côté de l'oxygène, délaissant le côté opposé.
On appelle polarité de la molécule d'eau, le fait de présenter ainsi une extrémité chargée positivement et l'autre négativement.
Une première conséquence est l'extraordinaire pouvoir de solvant dont elle fait preuve. En dissolvant une très grande majorité de substances, elle favorise les réactions chimiques entre elles.
Un exemple est le cycle de l'eau sur toute la surface terrestre : l'eau des océans s'évapore dans l'atmosphère, puis elle retombe sur les continents sous forme de précipitations. En ruisselant, elle dissout les minéraux, dont des composés carbonés. Enfin, elle retourne dans la mer, chargée des nutriments qui vont alimenter la vie. En transportant une grande quantité de carbone et de calcium, elle permet à la myriade des petits organismes de plancton de fabriquer leur squelette de calcite. En mourant, ils se déposent au fond des océans et s'enfouissent. C'est un des principaux mécanismes de réduction du gaz carbonique de la planète, et donc, de régulation du climat.
L'eau est très efficace pour stocker la chaleur ou le froid. Ainsi, nos océans stabilisent la température sur la planète. Sans cette propriété (une chaleur spécifique très élevée) la Terre présenterait peut-être comme Mars, des températures variant de -143°C à 20°C, selon les endroits et les heures !
Elle échange très efficacement la chaleur, ce qui renforce ce rôle stabilisateur. Cette propriété (une forte conductibilité thermique) n'est égalée par aucun autre liquide connu. Nous en tirons profit quotidiennement dans nos casseroles, notre chauffage central ou nos centrales nucléaires. Au niveau de la planète, les échanges de chaleur forment de grandes masses d'eau dans les océans, tel le Gulf Stream, qui fait remonter les eaux chaudes du sud vers le pôle Nord. Nous devons à ce courant le climat stable et tempéré qui a permis à la civilisation européenne de se développer considérablement.
Autre qualité unique de l'eau : il faut beaucoup d'énergie pour l'évaporer. Vous vous en rendez compte si vous voulez complètement évaporer une casserole d'eau. Cette propriété (une chaleur spécifique de vaporisation élevée) lui confère un fort pouvoir rafraîchissant quand elle s'évapore, une qualité exploitée par notre espèce depuis les premiers Homo issus des australopithèques. Ils sont devenus très efficaces à la course en abandonnant leur fourrure et en développant un système de transpiration performant. Aujourd'hui, en dehors du cheval, très peu de mammifères sont aussi endurants qu'un homme à la course !
La vie repose grandement sur l'effet hydrophobe. Toutes les substances ne sont pas compatibles avec la forte polarité de l'eau, en particulier les lipides. Leur répulsion pour l'eau est universellement utilisée par les êtres vivants, notamment pour former leurs membranes. On pourrait aller jusqu'à dire qu'un organisme vivant est un immense réseau de membranes. L'effet hydrophobe a certainement joué un rôle fondamental à l'origine de la vie : certains lipides comme les acides gras, forment spontanément des membranes et des vésicules. De là ont pu naître les toutes premières protocellules, il y a 3,8 milliards d'années.
Enfin l'eau est le seul liquide dont le volume s'accroît lors de la solidification. À l'état solide, la glace adopte une structure tétraédrique formant un angle très légèrement plus grand que celui de la molécule isolée. Cette distorsion imposée à la glace conduit à cette propriété étrange qui fait flotter les glaçons dans votre verre, mais plus fondamentalement elle a peut-être permis à la vie d'apparaître au fond des océans : sans elle, toutes les glaces terrestres se seraient accumulées au fond des mers et la calotte glacière du pôle Nord ne se serait pas formée.
Toutes ces caractéristiques singulières de l'eau paraissent faites pour que se développe la complexité. On peut se demander d'où vient une telle coïncidence. Son émergence repose sur les lois et les constantes de la physique qui, dès lors, semblent particulièrement bien réglées.
Cette question rejoint le problème de l'ajustement fin : de manière très générale, les astrophysiciens se sont aperçu qu'un univers aussi riche et stable que le nôtre ne pouvait exister que si les curseurs des constantes fondamentales étaient très finement positionnés. Sans doute la plus grande question que pose la science contemporaine…